多肽的固相合成|多肽固相合成技术( 二 )
缩合试剂主要有:碳二亚胺型,鎓盐型(Uronium)
碳二亚胺型
主要包括:DCC,DIC,EDC.HCl等 。采用DCC进行反应,由于反应中生成的DCU,在DMF中溶解度很小,产生白色沉淀,所以一般不用在固相合成中,但是由于其价格便宜,在液相合成中,可以通过过滤除去,应用仍然相当广泛 。EDC.HCl因为其水溶解性的特点,在多肽与蛋白的连接中使用比较多,而且也相当成功 。但是该类型的缩合试剂的一个最大的缺点,就是如果单独使用,会有比较多的副反应,但是研究表明如果在活化过程中添加HOBt,HOAt等试剂,可以将其副反应控制在很低的范围 。
鎓盐型
鎓盐型缩合试剂反应活性高,速度快,现在使用非常广泛,主要包括:HBTU,TBTU,HATU,PyBOP等 。该试剂使用过程中需要添加有机碱,如,二异丙基乙胺(DIEA),N-甲基吗啉(NMM),该试剂加入后,才能活化氨基酸 。
固相合成过程
1、羟基树脂为载体的合成方法(Wang树脂为例:图1)
Wang树脂、PAM树脂、HMPA树脂、Sasrin树脂等均在Linker结构中含有苄醇基 。多数情况下把预制的N一保护氨基酸的对称酸酐及催化剂DMAP(对二甲氨基吡啶)与羟基树脂一起反应 。在这种成键反应中 。DMAP是必需的,但也由此带来一些麻烦 。例如,当某些位阻较大、反应活性较低的Fmoc-氨基酸需要较长的反应时间,而且DMAP的纯度又不理想时 。会发生部分Fmoc基被脱除,生成部分二肽的麻烦 。更常见的危险是当Cys及His作为C端第一个氨基酸与羟基树脂反应时,DMAP往往使这两种氨基酸发生消旋化 。对此,解决办法是改用Cl-Trt树脂与这两种氨基酸键合,同样可以生成酯型Linker 。另一种解决办法是用MSNT试剂[Fra I388, Ren 1998],可以有效地免除Cys, His与多种羟基树脂键合时的消旋化危险 。
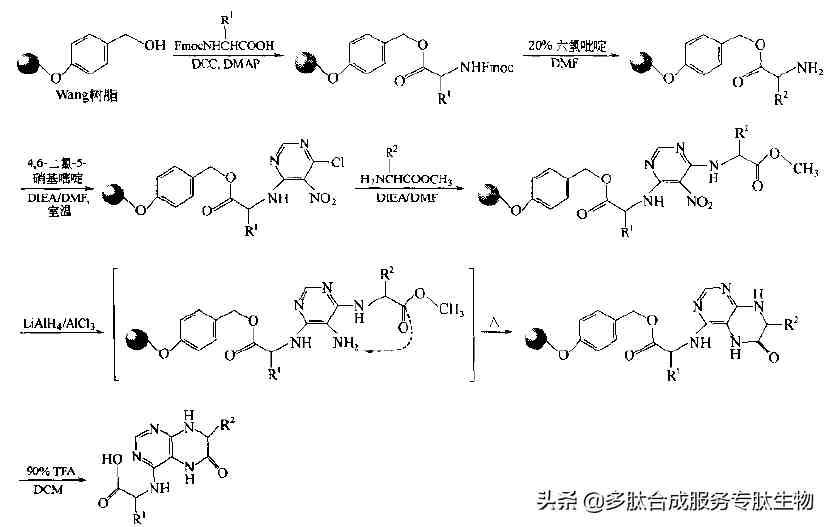
图1 固相多肽合成
2.以三苯甲基树脂树脂为载体的合成方法(图2)
三苯甲基(trt)树脂含有三重苄基结构,因此反应活性极高 。一般用等摩尔量的保护氨基酸及4倍量的DIEA与Trt树脂混在二氯甲烷中,室温反应30-12Omin即达完全 。对于未反应完全的位点,可用甲醇封住位点 。基于Trt Linker的温和键合及温和裂解特点,在此种树脂上进行肤片段缩合及全保护基肤片段制备是较理想的方式 。

图2 固相多肽合成
FMOC固相合成Glu-Trp
3以氨基树脂为载体的合成方法
MBHA树脂、PAL树脂、Knorr树脂、Rink-NH2树脂等均在Linker中含有可与羧酸反应的氨基 。C端第一个氨基酸与之键合的反应条件与接肽循环中的操作完全相同 。如果以DCC为缩合剂,一般先将N-保护氨基酸与DCC、HOBT混于溶剂(DMF、THF、百思特网DCM等)中,生成氨基酸的HOBT活泼酯,放置3-5h,待活化反应基本完全后滤除副产物DCU沉淀,把羧基活化组分溶液与氨基树脂混合进行键合反应 。此步反应有两点事项值得注意:①多数氨基树脂的氨基并非以游离状态出售 。有的氨基是以盐酸盐的形式,有的则带有临时保护基(如Fmoc , Boc等),因此在与C端第一个氨基酸键合之前必须进行相应的中和或脱除临时保护基的处理;②氨基酸活化组分的用量应大大高于氨基树脂组分,一般的摩尔比为(2-5):1,目的是使键合反应接近100% ,因为未被酰化的氨基树脂无法从产物中清除出去 。使用大大过量的构件是所有固相有机合成的共同之处 。
除了DCC之外,其他常见的缩合剂还有DIC、EDC、EEDQ、HBTU等 。
- 私人影院|私人影院可以看上映多久的电影
- 私人影院|私人影院会放映正在上映的电影吗
- 武汉|武汉樱花5月还有吗
- 武汉|武汉樱花在哪个大学
- 武汉|3月份武汉的樱花开了吗
- 身体乳|果酸身体乳怎么样,护肤效果好的身体乳排行榜
- 身体乳|身体乳哪个牌子的补水保湿效果好,身体乳排行榜
- 面霜|好用的面霜公认最好用学生党,口碑最好十大面霜排行榜
- 女性统治者|世界十大女性统治者,世界历史上的女性统治者
- 长高|十个长高的科学方法秘诀 怎样长高最快最有效
