电化学反应|电化学桑德迈尔反应
电化学反应(电化学桑德迈尔反应)
“桑德迈尔反应(Sandmeyer reac百思特网tion)”是有机化学中著名的人名反应,是通过重氮盐将芳香胺转化为芳香卤化物的重要方法,1884年由瑞士化学家Sandmeyer首先报道(T. Sandmeyer, Ber. Dtsch. Chem. Ges., 1884, 17, 1633-1635),在当今的基础科学研究和工业生产中具有广泛的应用 。然而,Sandmayer反应需要消耗化学计量的金属铜,由此带来成本较高和环境不友好等一系列局限 。一百多年来,有关桑德迈尔反应的延伸研究得到不断的丰富和发展,但新策略的研究仍具有重要意义 。
自从1848年Kolbe阳极氧化反应发现以来,电化学已经发展成为一项重要的技术,具有十分广泛的应用 。电化学生产己二腈和葡萄糖酸钙都是产量巨大的工业应用实例 。由于电势对电子转移具有强制作用,一些在常规化学反应中难以得失电子的反应物在电化学中可以很容易地得失电子,进而充当氧化剂或者还原剂,因此电化学反应通过正确的设计可以避免使用常规化学反应中传统意义上的氧化剂/还原剂,具有绿色、环保、温和的特点 。
最近,北京大学的莫凡洋课题组报道了电化学的桑德迈尔反应,以电为驱动力在阴极还原芳基重氮盐得到芳基自由基,进而与各种卤化试剂反应得到芳基卤化物 。相关工作发表在Chemical Science 上 。
作者首先分析了电化学实现桑德迈尔反应需要克服的三点问题 。其一,重氮盐可以在电极上发生双电子还原形成芳基阴离子,并进一步质子化得到还原产物;其二,芳基自由基可以与其他芳香烃反应(Gomberg-Bachmann)或与另一个芳基自由基反应生成偶联产物;其三,芳基自由基也可能直接与电极表面发生作用,改变电极表面的理化性质,并降低电化学过程的效率 。为了避免上述问题,作者提出以下两点解决方法:首先,通过调节电流来控制芳基自由基产生的速率,减少副反应的发生;其次,选择活性适宜的卤化试剂来快速捕捉新生成的芳基自由基 。这是电化学过程实现桑德迈尔反应的关键(图1) 。
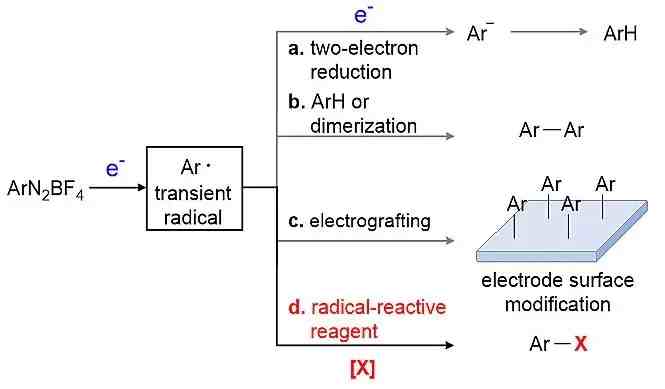
图1. 问题与解决办法 。图片来源:Chem. Sci.
作者以溴代反应为例,使用NBS作为溴化试剂,经过尝试,筛选出的最优条件为:使用体积比为5:1的MeOH/DMF作为混合溶剂,Bu4NClO4作为电解质,使用铂网电极在10 mA的恒定电流下电解3小时,产物2a得到83%的GC收率 。他们同时设计了其他条件均相同但不通电流的控制实验,反应的产率显著降低(20%,延长至15小时可提升至31%),表明所需产物主要由电化学反应过程获得 。此外,作者发现二碘甲烷(CH2I2)是优秀的碘化试剂 。与溴化和碘化相比,由于氯的电负性较高,氯化过程相对困难 。作者尝试了阳极氧化氯离子生成氯自由基的方法,使用简单的无机盐LiCl,泡沫镍作为阴极,可以较好地实现氯化反应 。同时,他们也将该反应扩展到使用NaBr作为溴源的溴化反应 。这种原位在体系中产生高活性的反应物种是电有机合成的一大优势 。
他们还对底物的适用范围进行考察,碘化、溴化、氯化反应均得到了良好至优秀的收率,具有良好的官能团兼容性 。总体而言,带有吸电子基团的底物可以得到更高的收率 。部分底物采用简单的NaBr、LiCl等无机盐作为卤化试剂,是该方法的一个亮点 。
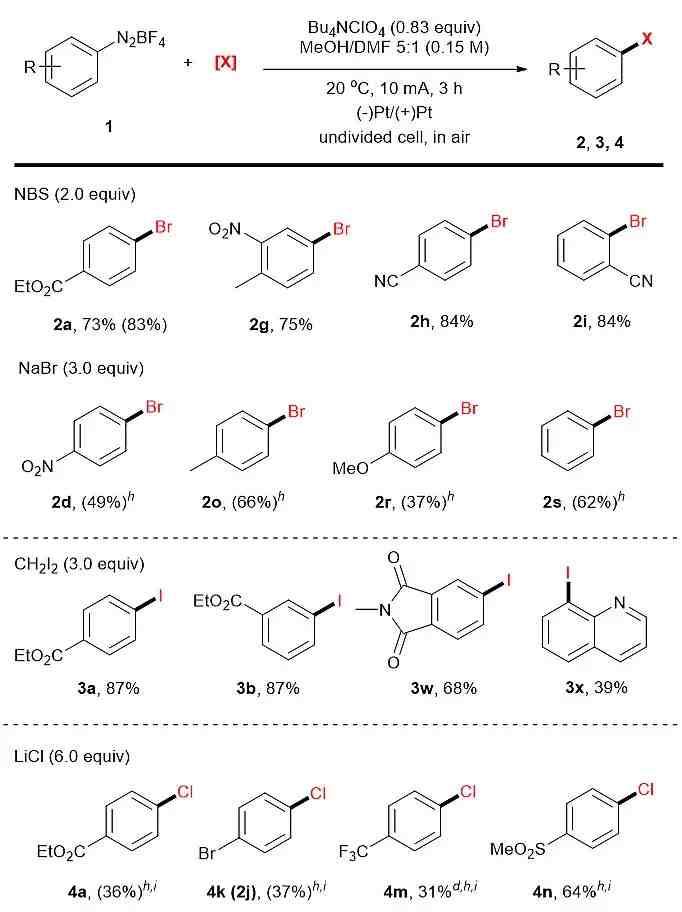
图2. 电化学重氮盐卤化反应底物适用范围的考察 。图片来源:Chem. Sci.
除了直接使用重氮盐作为底物进行反应外,作者研究了原位生成重氮盐的电化学卤化反应 。他们以芳香胺作为底物,在有机相中进行原位重氮化后直接加入卤化试剂电解,通过一锅法完百思特网成卤化反应,收率较高(42-83%) 。该一锅法也能够兼容许多官能团,如硼酸酯、酰胺和吲哚等 。
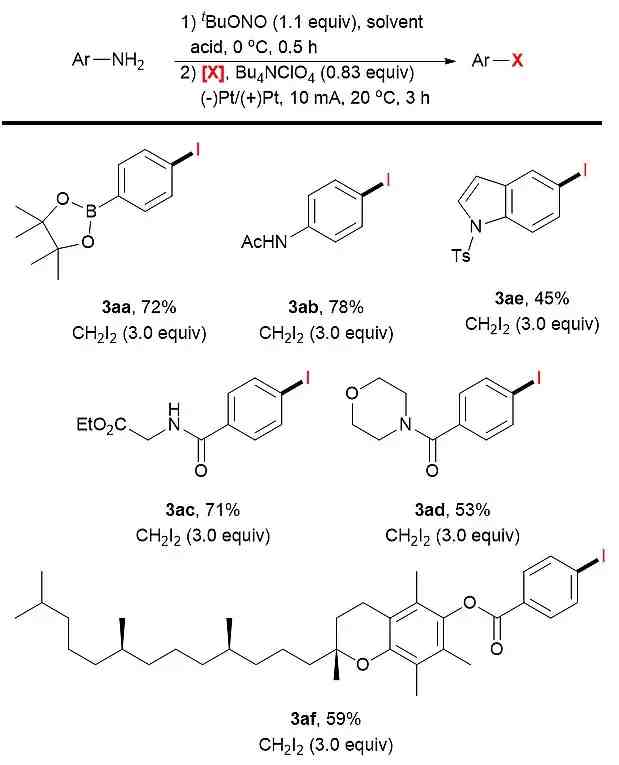
图3. 电化学苯胺卤化反应 。图片来源:Chem. Sci.
除此以外,作者使用廉价的大尺寸石墨板作为阴极进行3 g规模的放大实验,溴化和碘化分别得到了76-80%的收率,证明了该反应具有很高的实用价值 。
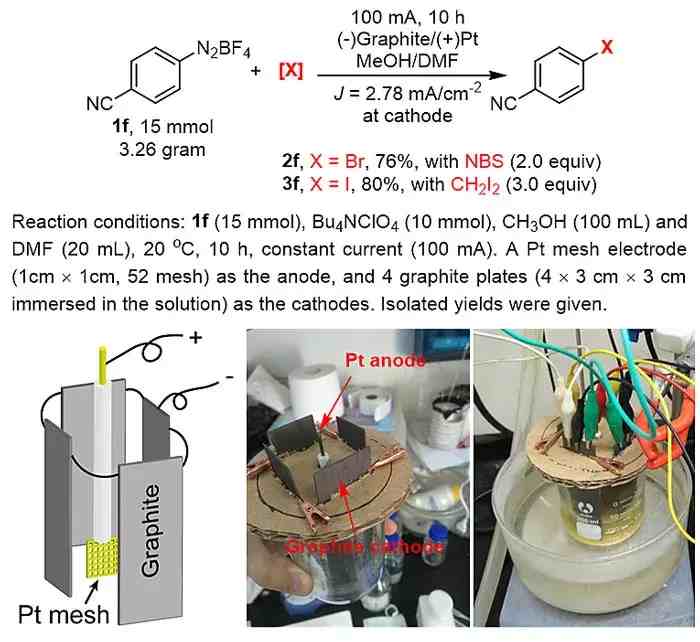
图4. 3 g量级规模反应的电化学装置 。图片来源:Chem. Sci.
最后,作者通过循环伏安法以及一系列控制实验等方法对该反应的机理进行了详细的研究,特别是应用了原位电子顺磁共振(EPR)实验方法 。EPR技术是研究自由基的重要方法,作者采用自行设计的装置原位跟踪反应过程中产生的自由基种类以及浓度 。如图5所示,他们将两根铂丝从上下两端分别通入扁平池,并将反应液置入扁平池中,使用电子顺磁共振仪每隔30秒记录一次反应体系的EPR信号(反应b的EPR信号随时间的变化见图6) 。由于有机自由基通常寿命极短,无法直接检测,因此反应体系中均加入了PBN作为捕获剂 。
- 私人影院|私人影院是自己选电影吗
- 私人影院|私人影院可以看上映多久的电影
- 私人影院|私人影院和电影院能同步上映吗
- 私人影院|私人影院会放映正在上映的电影吗
- 影院|私人影院有摄像头监控犯法吗
- 春节电影|2022年十大春节档电影 2022春节上映电影
- CSM收视率|63城2022年2月17日1930-2200含央视电视剧收视率排行榜
- CSM收视率|63城2022年2月17日电视台全天收视率排行榜
- ccdata收视率|2022年2月17日CCData全国网电视剧收视率排行榜TOP30
- ccdata收视率|2022年2月17日CCData全国网电视台收视率排行榜TOP30
